ˎ��������һ�N���N�����Ƴɵİ��b�M���M�϶��ɣ�ˎ���Ŀ������|�����ƺ���;�M�з��
�����|��ɷ֞�����������������մ�����z�������缈��������ȣ�Ҳ�����ɃɷN��ɷN���ϵIJ��Ϗͺϻ�M�϶��ɣ���ͺ�Ĥ���X�ܽM���w�ȣ���
���õ������ˎ������ˎ�õ��ܶȾ���ϩ���ۄ�ƿ���ڷ����wˎ�ø��ܶȾ���ϩƿ���۱�ϩݔҺƿ�ȣ�
���õIJ����ˎ�������c�}����ݔҺƿ������貣����ƿ����������ע�䄩ƿ�ȣ�
���õ����z�ˎ������ע��Һ���Ȼ��������z����ˎ�úϳɾۮ����ϩ�|Ƭ���ڷ�Һ�wˎ�ù����z�|Ƭ�ȣ�
���õĽ����ˎ������ˎ���X�����F�Ƶ�����ͺС�
����;�����Ʒ�ɷ֞�ݔҺƿ������Ĥ�����������ƿ��ˎ�ã�ע�䄩���ڷ��������Ä��ͣ�ƿ���ܡ��w����ˎ���z����ˎ���A���ע������ˎ�õ���(�ǡ���)��ƿ��ˎ��ӲƬ(Ĥ����ˎ���X����ˎ��ܛ��ܣ��У���ˎ�Ç����⣩�F���ã��y�T���ޡ�Ͳ����ˎ�ø���ȡ�
ˎƷ���b�����cˎ����������ָˎƷ���b�����cˎ��֮�g�l���w�ƻ������ȬF����������ˎƷ���b��횾߂������֮һ��ˎƷ���b���ϵ��|���������PˎƷ�|����ˎƷ�|�����Ʋ���ֻ�����ڽK�aƷ����Ҫע���������a�^�̿����Լ�ˎ���Ƅ��и��P�IҪ�ش��ڵĝ����L�U�Ϳ��܌�ˎƷ�|����Ӱ푡���ˣ���ˎ��I��ˎ�������a��I��횿���ˎƷ�Ͱ���֮�g�������ԣ��_��ˎƷ�b�ڰ��b���Ϻ��l���w�ơ��B�����g����r���Ա��CˎƷ��Ч�Ժͷ����ԣ��Ķ����χ�����ˎ��ȫ��
һ�����PҎ�����˜�
2015�桶�Ї�ˎ�䡷Ҏ����ˎ�����cˎ����������о����x��ˎ���ĵĻ��A��ˎ���Ƅ����x��ˎ���ĕr����M��ˎ�����cˎ����������о���
ˎ�����cˎ���������ԇ���]���͵��L�Uˮƽ��ˎ���cˎ��������õĿ����ԣ���1)��һ�㑪�������ײ��փ��ݣ�
��ˎ���Č�ˎ���|��Ӱ푵��о�������ˎ���ģ���ӡˢ�������ӄ���������w��С���ӻ������Լ��ӹ���ʹ���^���Юa���ķֽ���ȣ�����ȡ���w���о�����ȡ���w���о��Y���Ķ���W�u����ˎ���cˎ����֮�g�l�������Ŀ����ԣ�ˎ����Գɷֻ������o�ϱ�ˎ�������������յ���r�̓�������ݳ��Լ������ĝB�ȣ�
��ˎ�ˎ����Ӱ푵��о������콛���bˎ���ˎ���������ԡ������Լ��|����׃����r���粣��������ÓƬ���z��׃�εȣ�
�۰��b�Ƅ���ˎ����|��׃����ˎ�ﷀ���ԣ�����������ԇ���L��ԇ�ˎƷ�|����׃����r��
Ŀǰ��ˎ�������������P�˜ʞ顶���b����ԇ��.�����ԡ�����GB/T 16265-2008 ������
ԓ�˜�Ҏ���˰��b���������Ե�ԇ�����m�������в����g���������о���
���Ͱ��b�����c�����b�Ľ��١����ϻ��������w���ϣ�
������P���b�����c�����b�Ľ��٣�
������P���b�����c�ɟ��İ��b���ϣ�
Һ�B����Һ�B�Ʉ������ϡ�Ϳ���c�����o�Ľ����c�������w���ϡ�
�����z�y��һ�����
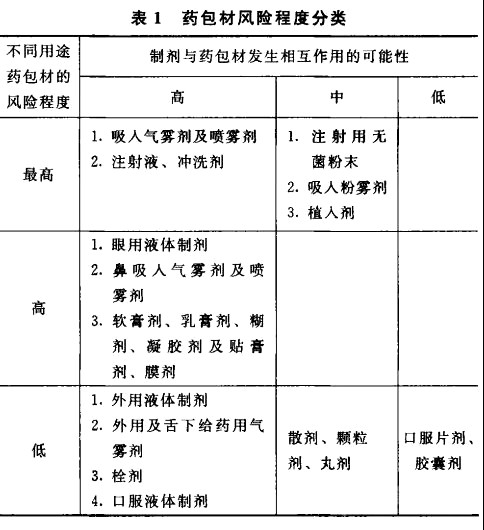
��һ�����_�JˎƷ�İ��b�M�����ɷ�
ˎ���ĵIJ��ϕ���ˎƷ�ķ���������Ҫ���ã�Ҳ��ֱ��Ӱ���ˎ�İ�ȫ�ԣ�ˎ���ij��÷N������ϡ����������ٺ����z���������ˎ���ijɷ��о���ϩ���۱�ϩ�ȷN��ʶ���ͬ�N�ˎ���ijɷֲ���Ҳ��һ�£����ȴ_�Jֱ�ӽ��|ˎƷ�İ��b�M�����ɷ֡�
�ڶ����������˽���b�M���IJ���
ˎ����һ�����r�²����dž�һ�ĽM�������Ƕ�N�N�ˎ�����ʹ�ã�������Щע��ˎ�������ˎ���ľͰ��������١�����Ҳ�п��������ϣ������҂��б�Ҫ��ˎ���ĵ�ÿһ���M�������M�з����˽⡣
���b�M���cˎƷ�Ľ��|��ʽ�c���|�l���Լ�ˎ���ĵ��������a��ˇ�^�̣��҂���Ҫ����㵽�Ŀ��������Ȼ������P�Y���ṩ�o�z�y����
����������ȡˎ�������c�Ŀ�о�
�@һ������ˎ���������Զ���ʮ����Ҫ����Ҫ��ȡ�о���̎��ˎ���Ę�Ʒ���x����ȡ�܄��Լ��_�J��ȡ�l�����Ŀ��ͨ�^������ȡ�о����Ԍ����M���b�e�z�y���A�yˎ���ĝ��ڵĿɽ����
���IJ����о�ˎƷ�cˎ���ĵ������
ˎƷ�cˎ���ĵ�������о����M��ˎ���������ԙz�y�ĺ��IJ��֣���Ҫ��ͨ�^�w�ƌ����������M�������{ԇ�z�y�Ŀ�ĘO�˗l���������r�g���ض������nj��o�ϵĺ�������A�ȵȗl��������ˎƷ���к����\ݔ�����桢ʹ�õȭh���£���ˎƷ�����ķ����ԺͰ�ȫ�ԡ�
���岽���u��ˎ�����cˎƷ��������
ͨ�^����ȡ�о���ˎ���ĵ�������о��£����Ե�֪ˎ���ĺͿ���ȡ������P����Ч������Ϣ�������@Щ��Ϣ���Ե�֪��ˎ�����Ƿ����ˎЧ�a��Ӱ푡���ˎ���o��������Ӱ푣��Ƿ���a��������Ķ���ˎƷ�|���a��Ӱ푣��Ķ��ó�ˎƷ���cˎƷ�������Ե��L�U�u�r��
��Ȼ߀��һ�c�҂���Ҫע�⣺Ӱ�ˎ���������ԙz�y�����c�����кܶ࣬����ˎ����Ҏ���С����͡�̎����ʽ�Լ�ˎƷ���|�ȣ���ˎ���������a�^����Ҳ��Ҫ�M����ϴ���̎�����@Щ���Ǽ{����ˎ���������ԙz�y�ķ���֮�ȡ�














 ��ǰ������棺
��ǰ������棺