һ�����係���ĸ���
1�����係��
ʳƷ�z�ӽ��^̎������һ���l�������B�������B���ɷ֡����B�ضȺ͕r�g��pH���������|�ȣ�������1mL����1g���z�����γɾ���Ŀ�����
�����Ҙ˜ʷ���Ҏ��������������r�£�37�����B48h������ƽ��Ӌ����֬ƽ�������L�ļ������係�������ԅ�������������������I�BҪ����Լ������Мصļ��������ڬF�Зl�����ܝM�������������y�Է�ֳ���L��������係��������ʾ���H�е����м������������係�������܅^�����м����ķN������Еr���Q���s���������������ȡ�
2����������
��������ָһ����������e��ʳƷ��Ʒ�����^�m����̎�������@�R�������M��ֱ��Ӌ�������а������N���������δ��ʧ������������������Ҳ�Q����ֱ���@�R����
ͨ����1g��1mL��1cm2��Ʒ�еļ�����������ʾ��
3�����係����ʳƷ�l���|���u�r�е����x
��1��ʳƷ�м��������ɷ�ӳԓʳƷ����Ⱦ�ij̶�
���r��ʳƷ�Ȳ�һ���Ǜ]�л�����м����ģ������������Ⱦ��r��ͬ��ʳƷ��������Ⱦ�Ķ��پ�������ͬ��ʳƷ�м�������Խ�࣬�f������Ⱦ�ij̶Ⱦ�Խ���أ�Խ�����r�������w�������{Խ���෴��ʳƷ�о���Խ�٣��f��ԓʳƷ����Ⱦ�ij̶�Խ�p��ʳƷ�l���|��Խ�ã������w����Ӱ�ҲԽС��
��2��ʳƷ�м����������A�yʳƷ�ͷų̶Ⱥ͕r�g
һ���v��������Խ�٣�ʳƷ�ͷŕr�gԽ�L���෴��ʳƷ�ͷŕr�g��Խ�̣�������0�汣��ţ�⣬���係����103cfu��cm2�r���ɱ���18�죬�������係������l05cfu��cm2�r�tֻ�ܱ���7�졣���⣬��0�汣���~�r�����係����105cfu��cm2�r�ɱ���6�졣�����係����103cfu��cm2�r�t�ɱ���12�졣
��3��ʳƷ�м��������ɹ��y��ʳƷ������r
һ���J���ճ�ʳƷ�Ļ������104��107cfu��g������������_��108cfu��g�t���J��̎�ڳ��ڸ����A�Ρ����磬��ļ��ݣ�Ƥ�w����ļ������ɵ͵�1.5��103cfu��cm2�����ӹ����R�ϙz�y���_3.5��104cfu��cm2�������䔵��107cfu/cm2�r��ʾ�_�ѽ��������u��ļ������_108cfu��cm2�r���К�ζ��׃ճ��
һ���v��ʳƷ�м�������Խ�࣬�t�����ٸ���׃�|�^�̵��M�̣�������������ʳ���ߵIJ���������
�������係���z�y����
���係���ij�Ҏ�z�����係���ij�Ҏ�z��(GB4789��2-2016)��
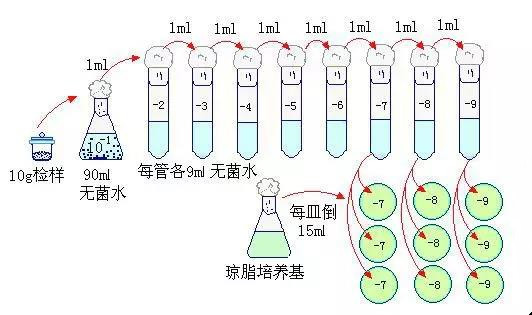
��������һ���������Ʒ��ϡጡ����Aעƽ�����B48��24��С�r����Ӌ����档
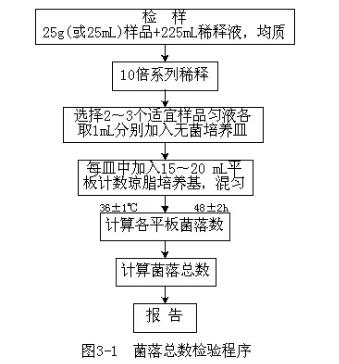
1����Ʒ��̎����ϡ�
��1����������
���ԟo������ȡ�z��25g����25ml)������225mL��������}ˮ������ϡ�Һ�Ĝ������ƿ�ȣ�ƿ���A���m�������IJ�����)���������ȣ��������Ҫ����ĥ�Ƴ�1��10�ľ���ϡ�Һ��
���w�z���ڼ���ϡ�Һ������Ü�����|������8000~10000r/min���ٶ�̎��1min���Ƴ�1��10�ľ���ϡ�Һ��
����1ml���������ȡ1��10ϡ�Һ1ml���عܱ�����ע�뺬��9ml��������}ˮ������ϡ�Һ��ԇ�܃ȣ���uԇ�ܻ�Ͼ����Ƴ�1��100��ϡ�Һ��
����ȡ1ml������ܣ�����헲��������10���f��ϡ�Һ�����ÿ�f��ϡ�һ�μ��Q��1֧1ml������ܡ�
��2���o������
�����б���С��o���������ĸ�����ò�������������ȫ����ġ����ü�������ӵ�����Ҳ����M������̎������Ʒ����а��b������75%�Ҵ��ڰ��b�_��̎���ú�ȡ�ӡ�
���������ڳ��������_���^����̎���ğo�����M�С���֬ƽ���ڹ����_��¶15��犣�ÿ��ƽ�岻�ó��^15�����䡣
��3���ɘӵĴ�����
��ϵ���w��Ʒ��ȡ�ӕr��������һ�c���˶�Ɏׂ���λ�����w��Ʒ��횽��^���|����ĥ��Һ�w��Ʒ횽��^��u���ԫ@�þ���ϡ�Һ��
4��ϡ�Һ
��Ʒϡ�Һ��Ҫ�ǜ�������}ˮ���еIJ��������}���_Һ����0.1��������ˮ�������ߌ�ʳƷ���ܓp���ļ���������һ���ı��o���á��猦���}���^�ߵ�ʳƷ�����u�ͣ��M��ϡጣ����Բ��Ü�����sˮ��
2���Aע���B
1����������
��1�������˜�Ҫ�����Ⱦ��r�Ĺ�Ӌ���x��2~3���m��ϡጶȣ��քe����10���f��ϡጵ�ͬ�r������ȡԓϡጶȵ�������ȡ1mLϡ�Һ�ڜ��ƽ���У�ÿ��ϡጶ����ɂ�ƽ��
��2��������46��ƽ��Ӌ����֬���B��ע��ƽ��s15mL�����D��ƽ��Ͼ���ͬ�r��ƽ��Ӌ����֬���B���A�����1mLϡ�Һ��������Ʒ���Ĝ��ƽ������հ��ա�
��3������֬���̺��Dƽ�壬��36��1���������B48��2h��ȡ��Ӌ��ƽ��Ⱦ��䔵Ŀ������ϡጱ���������ÿ�ˣ�ÿ��������Ʒ�������係����
��4���Aע�����B������46��ˮԡ�ȱ��أ��ض��^�ߕ�Ӱ푼������L���^�ͭ�֬��������������c��Һ��ֻ����oˮԡ������Ƥ�w�����^������C���ˡ�
�Aע���B������Ҏ����һ����12~20ml���ȣ�һ����15ml�^���m�ˣ�ƽ���^���Ӱ��^�죬̫�������ڸ��ѡ��Aע�r������ײ����г���������ײ���ȥ�������c���������Ӱ�Ӌ���^��
��5����ʹ��������ƽ���Ͼ���ֲ����zҺ����ƽ����M��Aע���B�������D��������ɂ��������D���z�ӏ��_ʼϡጵ��Aע���һ��ƽ�����Õr�g���˳��^20min���Է�ֹ��������������ֳ��
��6�����^�ͣ��ʶ����30�档���B�r�gһ���48h����Щ����ֻҪ��24h�����B����Ӌ�������B�䑪����һ���ĝ�ȣ���֬ƽ�����B48h�����B��ʧ�ز������^15����
��7�����˱���ʳƷ�е�С�w��������е��s�|�c��������l�����������ֱ棬��ͬ�r��һϡ�Һ�c��֬���B����ϵ�ƽ�壬�������B������4��h���з��ã��Ա�Ӌ���r�������^�졣
��ijЩ���ϣ����˷�ֹʳƷ�w���c����������壬���ڠI�B��֬�м����Ȼ������ĵ���TTC�������B�����ʼtɫ�����ڷքe��
3��Ӌ���͈��
��1����������
���B���r�g��Ӌ��ÿ��ƽ���ϵľ��䔵�����������^�죬��Ҫ�r�÷Ŵ��R�z�飬�Է��z©����ӛ�¸�ƽ��ľ��係�������ͬϡጶȵĸ�ƽ��ƽ�����䔵��Ӌ���ԭʼ��Ʒ��ÿ�ˣ���ÿml���еľ��䔵���M�Ј�档
��2��Ӌ��
���_Ҏ�����B�r�g��������Ӌ���������������Ӌ��������ƽ�������0��4�棬�����ó��^24h��
��3��ϡጶ��x���䔵��淽ʽ
����ֻ��һ��ϡጶ�ƽ���ϵľ��䔵���m��Ӌ�������ȣ�Ӌ��ɂ�ƽ����䔵��ƽ��ֵ���ٌ�ƽ��ֵ��������ϡጱ���������ÿ�ˣ���������о��係���Y����
�����Ѓɂ��B�mϡጶȵ�ƽ����䔵���m��Ӌ�������ȕr����ʽ��l��Ӌ�㣺
ʽ�У�
N�D��Ʒ�о��䔵��
��C�Dƽ�壨���m�˷������䔵��ƽ�壩���䔵֮�ͣ�
n 1�D��һ���m��ϡጶȽӷNƽ�傀��
n2�D�ڶ����m��ϡጶȽӷNƽ�傀����
d�Dϡ����ӣ���һϡጶȣ���
��������ϡጶȵ�ƽ���Ͼ��䔵������300���t��ϡጶ���ߵ�ƽ���M��Ӌ��������ƽ���ӛ䛞���Ӌ���Y����ƽ�����䔵�������ϡጱ���Ӌ�㡣
��������ϡጶȵ�ƽ����䔵��С��30���t����ϡጶ���͵�ƽ�����䔵����ϡጱ���Ӌ�㡣
��������ϡጶȣ�����Һ�w��ƷԭҺ��ƽ����o�������L���t��С��1�������ϡጱ���Ӌ�㡣
��������ϡጶȵ�ƽ����䔵������30~300֮�g������һ����С��30�����300�r���t����ӽ�30��300��ƽ�����䔵����ϡጱ���Ӌ�㡣
��4�����係���Ĉ��
�پ��䔵��100�ԃȕr�������������ˡ�ԭ�t�s�����Ã�λ��Ч���ֈ�档
���ˡ�ԭ�t�s��ȡǰ��λ���֣�������0����λ����Ҳ����10��ָ����ʽ����ʾ�������������롱ԭ�t�s���Ã�λ��Ч���֡�
��������ƽ���Ϟ����Ӿ�����o��Ӌ�����t���������ӡ�
�ݷQ��ȡ����CFU/g���λ��棬�w�eȡ����CFU/mL ���λ��档
4���eע��
��1����ͬϡጶȵľ��䔵���cϡጱ����ɷ��ȣ�ͬһϡጶȵĶ���ƽ��ľ��䔵�������ӽ�������ϡጱ������߾��䔵���٣�ϡጱ������;��䔵���ࡣ����F�淴�F�t��ҕ��z��еIJ��e���е�ʳƷ�Еr���ܳ��F�淴�F����������ϵȣ�����������z��Ӌ������������
��2����ƽ������朠�������L�r�����朠����L�ľ���֮�g�o�κ����@���ޣ��t������һ������Ӌ��������Ўחl��ͬ��Դ��朣��tÿ�l朾�����һ������Ӌ�㣬��Ҫ��������L��ÿһ��������_Ӌ��������Ƭ��������L��ԓƽ��һ�㲻�˲��ã���Ƭ����䲻��ƽ��һ�룬����һ���ֲַ����t���낀ƽ��ľ��䔵��2����ȫƽ��ľ��䔵��
��3����Ӌ��ƽ��ȵľ��䔵�^�ࣨ������ϡጶȾ�����300�r�������ֲ��ܾ���ȡƽ���һ���1/4Ӌ�����ٳ�������ϡጱ�������ԓƽ��ľ��䔵��














 ��ǰ������棺
��ǰ������棺